核酸熱穩定性分析 (Tm 分析)
基於核酸雜交的技術,例如 PCR 和 DNA 微陣列,在生命科學研究中不可或缺。此外,功能性核酸,包括核酸藥物和 siRNA (小型干擾 RNA),也逐漸獲得重視。在核酸的研究、發展以及應用中,熱穩定性分析 (Tm 分析) 不可或缺。
DNA 通常具有雙股螺旋結構。雙股包含分別以互補鹼基 G (鳥嘌呤 guanine) 和 C (胞嘧啶 cytosine) 與 A (腺嘌呤 adenine) 和 T (胸腺嘧啶 thymine) 組成的一個有意義股及一個反義股,而這些互補鹼基對由氫鍵連結在一起。溫度升高時會打斷氫鍵,雙股解離,並形成單股結構。這個現象稱為「解構」(melting)。
核酸在 260 nm 下會出現紫外線吸收峰,且在 260 nm 的吸收會隨解構發生而增加。相對於溫度升高以測量 UV 吸收時得到的資料曲線,稱為 UV 吸收解構曲線。除了 UV 吸收測量以外,也可在其他類型的測量中取得解構曲線,例如圓偏光二色性光譜分析和溫度測量。在解構溫度 (Tm) 下,雙股相對於單股的比率會變得相等。Tm 是核酸的熱穩定性指數,取決於各種條件,例如鹼基序列、鹼基數量、核酸濃度、溶劑條件 (鹽分組成、有機溶劑組成、pH)、錯配 (非互補的鹼基對)、核酸類似物 (人工核酸) 結構等。
和解構流程相反,溫度降低將造成單股核酸透過在互補鹼基對之間恢復氫鍵而形成雙股結構。這個現象稱為「雜交」。核酸的雜交會用於 PCR、DNA 微陣列、南方雜交、北方雜交和原位雜交等。此外,具有與 siRNA、反義核酸、反基因核酸、核糖體等相關之功能的核酸 (功能性核酸),也應用於多種領域,包括藥物發現研究、藥物和診斷。
核酸的熱穩定性是控制核酸結構、雜交和功能的重要因素;因此核酸的熱穩定性分析 (Tm 分析) 在這些領域中也不可或缺。
以下為核酸熱穩定性分析 (Tm 分析) 的簡單說明。在此假設 2 種不同單股 (A1、A2) 和雙股 (A1A2) 狀態之間有一個平衡狀態,且 A1 和 A2 的濃度相同。
A1 + A2 ⇔ A1A2 (1)
若雙股莫耳分率為 α,而核酸總濃度為 Ct,系統的平衡常數 K 如下所示。
K = [A1A2] / ([A1] [A2]) = 2α / ((1 - α)2Ct) (2)
在 260 nm 下觀察到的吸收 (Aobs) 如下所示。
Aobs = (εdsα + εss (1 - α)) CtL (3)
εds, εss 和 L 分別表示雙股莫耳吸收係數、單股莫耳吸收係數和光徑長度。
如圖 1 從實際測量取得的解構曲線所示,ε ds 和 ε ss 與溫度相關。 由於相較於轉變區域期間 (大幅吸光變化的區域),在低溫轉變前區域 (大幅吸光改變之前的範圍)
和高溫轉變後區域內,吸光變化大致為線性,ε ds and εss 以下列方式表示,其中 T 代表溫度。
εds = ads + bdsT (4)
εss = ass + bssT (5)
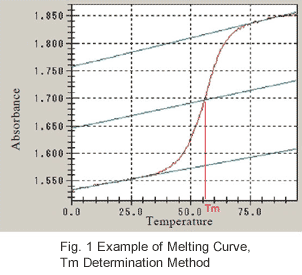
α = 1/2 時,溫度變成 Tm,這是用於從解構曲線決定 Tm (解構溫度) 的條件。如圖 1 所示,會相對於轉變前區域和轉變後區域決定基準線。接著畫出 2 條基準線的中位線,取得此線與解離曲線交叉點的溫度 (Tm)。
Gibbs 自由能變化、焓變化和熵變化,分別為 ΔG、ΔH 和 ΔSS,用於表示熱力學的基本原理,其中在莫耳比熱變化 (ΔCp) 為零時,可取得以下表示式。R 為氣體常數。
ΔG = ΔH - TΔS = -RTlnK (6)
將表示式 (2) 代換為表示式 (6),在溫度 T m下 α = 1/2 時,會取得以下表示式。
1 / Tm = (R / ΔH) ln(Ct / 4) + ΔS / ΔH (7)
樣品會在不同濃度下 (Ct) 製備,取得個別的 Tm 值,將 1/Tm 相對於 ln(Ct/4) 繪圖,可從取得的直線斜率和 y 軸截距決定 ΔH 和 ΔS。
島津為其多種雙光束 UV-VIS 分光光譜儀 (UV-1800/UV-2450/UV-2550 等) 提供 Tm 分析配件選項,可確保進行核酸的穩定熱分析。Tm 分析系統 (TMSPC-8) 包含一個電熱溫控 8 串聯微型容槽固定架、一個溫度控制器、一個 8 串聯微型多容槽 (光徑長度 10 mm、1 mm) 和專門設計的 Tm 分析軟體。8 個串聯容槽可同時進行最多 8 個樣品的熱解構分析。
下方顯示 Tm 分析資料以及熱穩定性效能分析結果的範例。
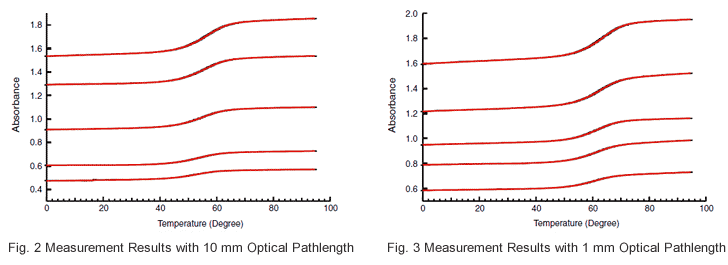
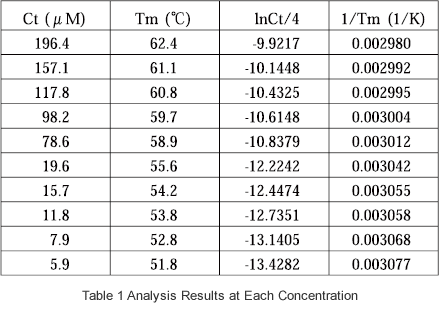
使用包含 GCGAAAAGCG/CGCTTTTCGC 的樣品,從具有不同濃度的 10 份樣品測量取得資料。濃度列於表 1。取決於樣品的吸收,使用光徑長度為 10 mm 或 1 mm 的容槽。取得的資料列於圖 2 和圖 3,且測量條件如下所示。
| Buffer | : 100mM Sodium Phosphate, 1M NaCl, 0.5mM EDTA, pH7.0 |
| Wavelength | : 260nm, 320nm |
| Temperature Range | : 0 to 95°C |
| Ramp Rate | : 1°C/min |
| Sampling Interbal | : 0.5°C |
| Waiting Time | : 30sec |
| Post-Process Annealing | : (95°C, 2min) |
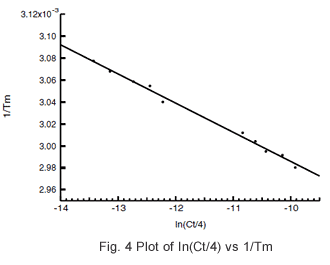
Tm 分析軟體用於決定每個濃度下的 Tm 值,並計算 1/Tm 和 ln(Ct/4)。表 1 的資料繪圖並取得圖 4 的線性。使用這條直線斜率和 y 軸截距,取得的 ΔH 和 ΔS 分別為 -74.6 kcal/mol 和 -202.9 cal/(molK)。
除了上述的 ΔH 和 ΔS 決定方法以外,也可以使用解構曲線非線性適配方法決定 ΔH 和 ΔS。
雜誌中說明多個 UV 相關主題,以及使用島津 UV 分光光譜儀的有用分析資訊及專技知識。


